MEME HASTALIKLARINDA TANI ve TARAMA
GİRİŞ
Meme kanseri önemli bir sağlık sorunu olmaya devam etmektedir. Epidemiyolojik olarak 70
yaşına kadar olan kadın popülasyonun %10’u meme kanserine yakalanmaktadır 1. Erken tanının
sağ kalım üzerindeki etkisi tartışmasızdır. Bu nedenle koruyucu hekimlik yönünden bakıldığında, kendi kendini muayene konusundaki eğitimin üzerinde özellikle durulmaktadır. Ancak meme kanserinin sağ kalım oranına kendi kendini muayenenin etkisini gösterecek kesin veriler bulunmamaktadır 2. Öte yandan meme ile ilgili klinik belirtiler nedeniyle hekime başvurular klinik uygulamada oldukça önemli sayıdadır. “Human maintenance organisation” (HMO) verilerine göre meme ile ilgili yakınmalar nedeniyle hekime başvurular son 10 yılda %16 oranına ulaşmıştır 2,3. Meme biyopsileri tüm cerrahi patoloji örneklemeleri içinde %5 oranında bulunmaktadır. Her ne kadar başvuran hastalardaki bir çok klinik semptom çoğunlukla benign meme hastalıkları ile ilişkili olsa da ayaktan başvuruların %4 ü kanser tanısı almaktadır 4. Görüntüleme yöntemlerinde sağlanan gelişmelere karşın klinisyen tarafından yapılan cerrahi girişimlerin %26’sı kanser varlığını göstermek amaçlı olmaktadır. Görüntüleme yöntemleri denilince akla ilk gelen mamografi olmaktadır. Tarama amaçlı mamografi sayesinde asemptomatik ve/veya palpe edilemeyen lezyonların varlığı saptanabilir hale gelmiştir.
Günümüzde tarama mamografileri ile birlikte fizik muayenenin meme kanserine bağlı mortaliteyi %25 azalttığı yönünde rasyonel veriler bulunmaktadır 5. Ancak sağlanan bir çok gelişmeye karşın, 50 yaşın altındaki hastalarda kanserin erken tanısı zorluğunu korumaktadır. Bunun sonucu olarak benign meme hastalıklarını taramaya yönelik yapılan girişimler psikososyal ve finansal maliyeti de göz önünde bulundurulursa özellikle maligniteyi ekarte etmek açısından önemini korumaya devam etmektedir 6. Bu durum göz önüne alındığında özellikle kanserin ekarte edilmesi ya da Dr.Hüsnü Göksel’in tanımı ile “memede kanser olmadığının ispatı” klinisyenin (cerrah-radyolog-patolog) temel ereği olmalıdır. Bu bölümde meme kanserinin klinik belirtileri ve fizik muayene teknikleri, meme görüntüleme, doku örnekleme yöntemleri (stereotaktik görüntüleme ve meme biyopsi, sitolojik ince iğne aspirasyon örneklemesi, duktoskopi), meme tümörlerinin biyolojik davranış özellikleri üzerinde durulacaktır.
1.1.Klinik belirtiler, anamnez ve fizik muayene yöntemleri
1.1.A. Klinik belirtiler
Meme hastalıklarında tanısal gecikme başlıca üç nedene dayanmaktadır. Bunlar ekonomik etmenler, kişinin kendisini ihmal etmesi ve psikolojik nedenlerdir. Bunlardan ilki sağlık güvencesi ile ilgili sorunlardır. İkincisi özellikle yaşlı hastalarda görülen ve ağrı oluşmadığı sürece hekime başvurmama eğilimidir. Psikolojik nedenlerin temelinde ise kadınların % 47’sinin meme dokusuna emosyonel olarak künt bir tavır sergilemeleri yatmaktadır7.
Yapılan araştırmalarda kliniğe başvuran hastaların %42’si kendi fark ettikleri kitle ile başvururken, cerrahın fizik muayene sırasında saptadığı kitle oranı %24 olarak belirlenmiştir8. Bu oran meme kanseri tanısının konmasında, cerrahın meme hastalıkları konusunda deneyimli olmasının önemini göstermektedir. Muayene sırasında cilt retraksiyonu, cilt ya da meme başında erozyon, meme başı akıntısı, meme başında inversiyon, meme cildinde ödem, hiperemi, ısı artışı saptanabilir. Özellikle hastalığın klinik evrelemesinin doğru yapılabilmesi yönünden Haagensen retraksiyon testleri klinisyen tarafından dikkatle yapılmalıdır ve bir diyagrama not edilmelidir (Şekil 1).
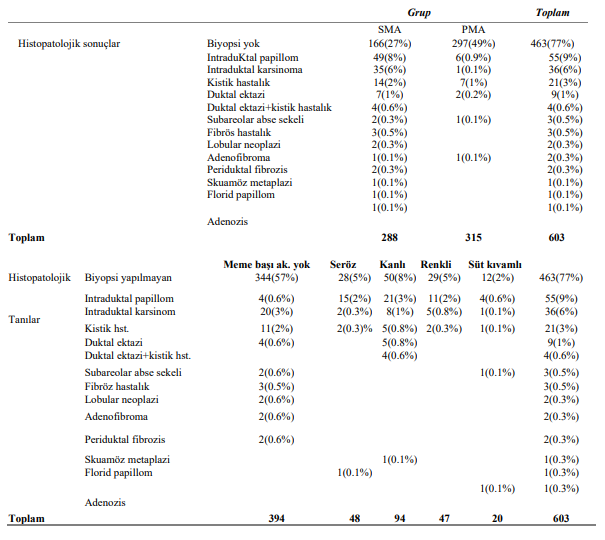
Haagensen retraksiyon testleri lokal ilerlemiş meme kanserinin tanısında halen çok önemli yer tutmaya devam etmektedir. Burada özellikle uzak metastazın olmadığı lokal ilerlemiş meme tümörlerinin tedavisindeki başarıda, tümörün biyolojik davranışında kişisel immünitenin rolünü de vurgulamak gerekmektedir. Fizik muayene sırasında “fossa aksillaris” ve “fossa supraclavicularis”in dikkatli muayenesi sadece kitle ile başvuran ya da kitle saptanan hastalarda değil, radyolojik görüntüleme ile kitle saptanmayan hastalarda da önemlidir. Çünkü meme kanseri %0.3-1 oranında “occult carcinoma” olarak kendisini gösterebilir 9. Bu nedenle bu anatomik boşluklardaki 5 mm ve üzerindeki lenf nodülleri özenli değerlendirilmelidir. Diğer yandan “American College of Surgeons” verileri, tarama amaçlı yapılan mammografilerle tanı oranının %36 oranında olduğunu bildirmektedir8. Menstrüel siklus ile ilgili olmayan büyüme eğiliminde olan kitlelerin meme kanseri olma olasılığı her zaman daha yüksektir. Meme başı akıntısı da kanser yönünden klinisyeni uyarması gereken belirtilerden biridir. Özellikle tek taraflı ve tek duktustan olan spontan meme başı akıntıları cerrahi girişim gerektirir. Kanlı meme başı akıntılarının en sık nedeni “intraduktal papillom”lar olup, kanser de kanlı meme başı akıntısına neden olabilir. Başkent Üniversitesi Tıp Fakültesi’nde Dr.Hüsnü Göksel’in 40 yıllık kişisel serisindeki 603 meme başı akıntısı olan hastanın özellikleri Tablo 1’de özetlenmiştir. Bu sonuçlara göre, seröz ve berrak meme başı akıntıları da kanser yönünden dikkatli olmayı subareolar eksplorasyon zamanlamasında dikkatli olmayı gerektirmektedir9. Bu nedenle meme başı akıntısı nedeniyle başvuran hastalarda akıntının vasfı mutlaka sorgulanmalıdır. Akıntının
olduğu duktusun belirlenmesi özel bir muayene şekli gerektirir ve değerlendirme deneyimli bir meme cerrahı tarafından yapılmalıdır.
1.1.B. Anamnez
Meme hastalıklarının tanı ve tedavisinin anamnez aşamasında memede saptanan bir kitlenin boyutu ve ne kadar süredir hasta tarafından fark edildiğine dikkat edilmelidir. Kitlenin kanser olduğunun ispat edilmesi durumunda ameliyat öncesi sistemik taramada metastaz da saptanmaması halinde, hastalığın iyi prognozlu olacağına hükmedilebilir. Meme polikliniklerine başvuran hastalarda meme ağrısı ikinci sıklıkta görülmektedir. Ağrı ile birlikte kitle varlığı ya da ağrının menstrüel siklus ile ilişkisi ayrıca sorgulanması gereken bir durumdur. Ayrıca sorgulamada erken menarş ve geç menopoz olup olmadığına da dikkat edilmelidir. Erken menarş ve geç menopoz meme kanseri riskini %30-50 oranında artırmaktadır. Bütün bunların yanında, meme kliniğine başvuran bir hastanın hormon alımı yönünden dikkatli sorgulanması gerekir. Özellikle hormon replasman tedavisi klinik olarak memede dolgunluk hissi ve hassasiyet oluştururken, mammografik duyarlılığı azaltır.
Aile öyküsü, meme kanseri gelişiminde kalıtımın majör risk faktörü olduğu göz önüne alınırsa büyük önem taşır10. Meme kanserlerinin % 7’si, over kanserlerinin ise % 10’unun otozomal dominant geçiş gösterdiği unutulmamalıdır. Özellikle BRCA1 ve BRCA2 genleri herediter meme kanserlerinde % 85 oranında sorumlu bulunmaktadır.
Kalıtsal over kanserlerinde ise BRCA1 için bu oran % 70, BRCA2 için ise % 20 olarak bildirilmektedir 10. Bu nedenle, 50 yaş altında birden fazla aile ferdinde görülen meme ve over kanserlerinde genetik test ve genetik danışma yarar sağlayacaktır. Değerlendirme tıbbi onkolog-jinekolojik onkolojik cerrah ve meme cerrahı-tıbbi genetik uzmanı tarafından bir konsey tarafından yapıldıktan sonra koruyucu mastektomi-koruyucu salpingooferektomikoruyucu hormonoterapiler yönünden hasta bilgilendirilmelidir. Meme ve over kanseri yönünden kalıtsal riskli hastalarda 20 yaşından itibaren 6 aylık aralıklarla meme cerrahı tarafından kontroller başlatılmalıdır. Öte yandan 25 yaşından sonra yıllık mammografi, 30 yaşından sonra da transvajinal ultrasonografi, Doppler inceleme ve CA 125 testleri eklenerek hastaların sorumluluğu üstlenmelidir.
Ayrıca hastanın öyküsünde lenfoma varlığının meme kanseri yönünden risk oluşturduğu bilinmektedir. Hodgkin hastalığı sonrası de novo kanser riskinin aynı yaş aralığındaki sağlıklı nüfusa göre 4.6 kat arttığı literatürde bildirilmektedir11. Özellikle 30 yaşın altında Hodgkin lenfoma tanısı alan hastalarda meme kanseri riski belirgin olarak artmaktadır. Burada özellikle tedavi sırasında alınan radyoterapinin predispozisyon oluşturduğu söylenebilir. Ayrıca hastanın önceden meme kanseri geçirmiş olması kontrlateral memede kanser gelişimi riskini artırmaktadır. Kliniğimizde yapılan bir çalışmada primer kanseri premenopozal dönemde saptanan hastalarda uzak metastaz oran primer kanseri postmenopozal dönemde saptanan kanser olgularına göre daha yüksek bulunmuştur12.
Meme hastalarının klinik değerlendirilmesinde önceden yapılan meme biyopsileri dikkatli sorgulanmalı ve yapılan biyopsi sonucunun histopatolojik olarak prekanseröz lezyonlar olup olmadığı dikkatli araştırılmalı, patolog ile de konsültasyon süreci sağlıklı işletilmelidir.
1.1.C. Fizik muayene
Günümüzde 40 yaşın altındaki sağlıklı kişilerde 3 yıllık aralıklarla önerilen muayene ile kontrolünün, 40 yaşın üzerinde yıllık yapılması önerilmektedir. Ancak bu görüş meme kanserinde genetik etmenlerin ortaya konması ile değişme eğilimindedir.
Meme muayenesine başlamadan evvel meme hastanın endişeli ve aynı zamanda çekinme duygusu ile yüklü olabileceği akılda tutulmalıdır. Muayeneden önceki görüşme sırasında ikinci bir kişinin varlığı hastanın cesaretlenmesi açısından yararlı olabilir. Meme hastalıklarının tanısının konmasında kendi kendine muayene tanısal sürecin bir aşamasıdır. Kendi kendine düzenli muayene yapan hastalarda benign bir meme hastalığı nedeniyle yapılan biyopsi oranı yapmayanlara oranla daha yüksek bulunmuştur13. Meme ile ilgili yakınma nedeniyle meme kliniğine başvuran hastalarda yaklaşık % 50 kadarında hasta tarafından memede herhangi bir anatomik anormallik fark edilemeyebilir. Bu rakamlar göz önüne alındığında, fizik muayenenin meme konusunda deneyimli bir cerrah tarafından yapılması gerektiği açıktır.
Fizik muayene inspeksiyon, palpasyon ve klinik evrelemede önemli olan “fossa supraclavicularis” ve “fossa axillaris”i içerecek şekilde yapılmalıdır. Hasta oturur pozisyonda iken her iki memede asimetri, kontür düzensizliği, ödem, eritem, renk değişikliği, meme başında retraksiyon varlığı gözlenmeli ve dikkatle not edilmelidir. Daha sonra hastaya her iki eli ile iliak kanatlar üzerine baskı uygulatılarak meme derisinde pektoral kasın kontraksiyonu sonrası cilt retraksiyonu olup olmadığı değerlendirilir. Bunun sonrasında her iki kol öne doğru uzatılarak ve yukarı kaldırılarak aynı işlem tekrarlanır. Bu şekilde retraksiyon testleri tamamlanır. Her iki “supraclavicular fossa” ve “axillar fossa” olası lenf nodüllerinin varlığını araştırmak için dikkatle palpe edilmelidir. Bu palpasyon muayenesi sırasında 5 mm ve üzeri herhangi bir lenf nodülü varlığı dikkatle kaydedilmelidir.
Hasta yatırılarak her iki memenin palpasyonuna devam edilir. Palpasyon muayenesi sadece iki parmak kullanmak suretiyle periareolar bölgeden memenin periferine doğru Langer çizgilerine paralel olarak yapılmalı, kitlenin kadranı ve büyüklüğü, hareketli olup olmadığı, sınırlarının düzenli olup olmadığı belirtilmelidir. Memenin periferine doğru gelindiğinde “tail of spence” veya “axillar abberan” meme dokusu varlığı gözlenmeli, bu dokuların içinde gelişebilecek maligniteler yönünden uyanık olunmalıdır. Bu konuda Başkent Üniversitesi Tıp Fakültesi Genel Cerrahi Anabilim Dalı’nda Dr.Hüsnü Göksel’in kişisel serisi oldukça önemli bilgiler vermektedir14. Bütün bu muayeneler sırasında elde edilen bulgular bir diyagrama detayı ile not edilmeli gerekirse ameliyat öncesi planlama için fotoğraf çekilmelidir.
1.2.Tanısal testler
Klinik belirtiler, anamnez ve fizik muayene bulguları değerlendirildikten sonra gerçekleştirilecek olan tetkikler non-invazif ve invazif olmak üzere ikiye ayrılabilir.
1.2.A. Non-invazif tetkikler
Mammografi:
Mammografi non-invazif bir tarama ve tanı yöntemi olmasına rağmen işlem sırasında uygulanan kompresyon özellikle oluşturacağı ağrı yönünden hasta memnuniyetsizliğine neden olan bir durumdur. Ancak kompresyon daha düşük radyasyon dozuyla daha sağlıklı görüntüleme yapılmasını sağlamaktadır. Deneyimli bir ekibin varlığı ve çekim işleminin prementrüel dönemde yapılmaması bu konudaki olumsuzlukları azaltabilmektedir.
Meme hastalıklarının tanısında mammografi bugün klinik uygulamanın vazgeçilmezi durumundadır. Düşük doz radyasyon kullanılarak yapılan bir tarama yöntemidir. Her mammografi işleminde, hastaya 0.1 rad radyasyon verilmektedir. Akciğer grafisi çekilirken hastanın maruz kaldığı radyasyon oranı 0.025 rad civarındadır. Genel olarak mammografi çekiminin memeyi kanser yönünden risk altına soktuğu yanlış bir kanı olarak yerleşmiştir. Literatürde tarama amaçlı mammografi yüzünden meme kanseri geliştiğine dair bir kanıt bulunmamaktadır15 Taramanın kanserin erken tanısında sağladığı avantaj ile mammografi çekiminde karşılaşılan riskin karşılaştırıldığı çalışmalar mevcuttur. Tarama mammografileri sayesinde 40-49 yaş arası kadınlarda meme kanserine bağlı ölüm riski %35, 50 yaş ve üstü kadınlarda ise %46 azaltılmıştır. Mammografiden dolayı maruz kalınan ölüm oranı lineer risk
ektrapolasyon eğrileriyle incelenmiştir. Buna gör 40-74 yaşları arasında yılık tarama amaçlı mammografi çektiren 1.000.000 hastada 18.000 hasta meme kanserine bağlı ölümden kurtarılırken, 21.6 hasta muhtemel radyasyona bağlı olarak kaybedilmiştir16 Aynı çalışmada yarar/risk oranı 875/1 olarak verilmektedir. Bu nedenle mamografinin özellikle palpe edilemeyen kanser lezyonlarının hastalık erken evrede iken saptanmasındaki katkısı tartışılmazdır. Mammografinin en yaygın kullanılan tarama testi olmasına rağmen asemptomatik hastalardaki lezyonların yaklaşık %8-%15’i rutin mammografilerle saptanmaktadır.
Toplumdaki bilinçlenmeye rağmen 50 yaş ve üstü kadınların ancak %15-20’si mammografi yaptırmaktadır. Fizik muayene ve mammografi palpe edilemeyen lezyonların tanısında sağladığı yardımla kanserin daha erken tanısını sağlamakta ve hastaların sağ kalımını olumlu etkilemektedir.
Mammografik tarama intervali meme tümörlerinin biyolojik davranışı ile ilintilidir. Burada tarama aralığını “lead time” kavramı belirlemektedir. Bu yaş gruplarına göre değişiklik gösterir. “Lead time” tümörün taramada saptandığı an ile klinik belirti verinceye kadar geçen süredir. Bu süre 40 yaş altındaki hastalarda 40 yaş sonrası hastalara göre daha kısadır. Geniş seri içeren çeşitli çok merkezli araştırmalarda, tarama mammografilerinin bu gerekçeyle 40-49 yaş arası kadınlarda yıllık olarak yapılması önerilmiştir. Bütün meme kanserlerinin %19’u 40-49 yaşlar arasında görülürken %5’ten azı 40 yaş altında, %0.3’ten azı 30 yaş altında görülmektedir. Bu nedenle tarama amaçlı mammografi 40 yaş altı kadınlarda bazı özel durumlar dışında önerilmemektedir.
Tarama ve tanı amaçlı uygulamalarda mammografinin endikasyonları belirlenmiştir. Palpe edilen tümörü olan hastaların yanısıra, asimetri varlığı, meme başı akıntısı, cilt retraksiyonu ve aksiller lenfadenopmegali mammografi ile değerlendirilmelidir. Mammografinin yanlış negatiflik oranı %10-15 civarındadır. Bu nedenle negatif mammogram varlığında özellikle premenopozal hastalarda fizik muayene bulguları önem kazanacaktır. Lobuler neoplazi, lobuler karsinom, intraduktal papillomatozis ve makroskopik kistik hastalığı olanlara düzenli aralıklarla mammografi çekilmelidir. Ancak asemptomatik hastalarda tarama amaçlı mammografiler 40-49 yaşları arasında 12-24 ay aralıklarla yapılırken, 50-75 yaş sonrasında da mammografi yine yıllık olarak önerilmektedir. Ayrıca 50 yaş altında yüksek riskli hastalara yıllık yapılmasına dair görüşler de bulunmaktadır.
Tarama amaçlı mammografiler 75 yaş sonrası hastalarda genel sağlık durumu ve yaşam beklentisi olduğu sürece yapılmalıdır. Zira yaşla birlikte hastalarda mammografi duyarlılığının arttığı, bu yaş grubunda erken tanı konduğu takdirde sağ kalım avantajı sağlayacak agresif tümör tipleri olabileceği unutulmamalıdır.
Mammografide saptanan kitle, mikrokalsifikasyon, “stellate” dansiteler, yapısal distorsiyon ve
mammografide interval değişikliği sonucu yapılan biyopsilerde %20-%30 oranında kanser tanısı konmaktadır. Tarama mammografilerinde maliyeti artıran ve hastada anksiyete oluşturan nedenlerin başında biyopsi önerisinin sıklığıdır. Pozitif kestirim değeri (PKD) malignitenin yakalandığı biyopsi oranını gösterir. Bu oran American Collage of Radiology verilerine göre %25-40 oranında kabul edilebilir olmaktadır17. Pozitif kestirim değeri 40-49 yaş, 50-59 yaş, 60-69 yaş ve 70 yaş üstü hastalarda sırasıyla %22, %35%, %45 ve %50 olarak verilmektedir18,19. Tarama testi olarak ultrasonografinin de kullanımı, hastanın düzenli aralıklarla meme cerrahı tarafından fizik muayene ile izlenmesi yanlış pozitif biyopsi oranlarını azaltacaktır. Yaş ile birlikte kanser insidansının arttığı göz önüne alınırsa 40-49 yaş arası hasta grubu özellikli bir yaş aralığını meydana getirir. Bu yaş döneminde kanser gelişimi hala agresif biyolojik davranış sergileyebilmektedir. Öte yandan fibroglandüler doku yoğunluğunun fazla olması nedeniyle mammografik duyarlık da bu yaş aralığında azalmıştır. Bu durum tarama mammografileri sonucu biyopsilerde PKD’ni olumsuz etkilemektedir. Sağlıklı bir sonuca varmak için mamografi dışında diğer görüntüleme yöntemlerine başvurulması 1.7 defa daha fazla olmaktadır.
Meme hastalıklarının tarama ve takip sürecinde önemli sorunlardan birisi de duktal karsinoma in situ (DKİS) lezyonlarıdır. Mammografinin tarama olarak kullanılmadığı dönemde memenin malign lezyonları içinde DKİS oranı %5 iken, günümüzde mammografinin yaygın kullanılmasıyla bu oran palpe edilemeyen kanser lezyonlarının %20-40 kadarını oluşturmaya başlamıştır. Halen uygun tedavi yaklaşımlarıyla DKİS saptanan hastalarda %99.5’ a varan sağ kalım oranlarına ulaşılmıştır. Yapılan çalışmalar, invazif duktal karsinom (İDK)’un DKİS lezyonlarından geliştiğini, ama her DKİS lezyonundan ise İDK gelişmediği yönündedir. Her hangi bir DKİS lezyonundan ne kadar süre içinde İDK geliştiği sorunsalı, tarama testleri ve takip programlarını zorlaştırmaktadır. Literatürde yapılan bir çalışmada memede biyopsi yapılan yerde 9.7 yıl içinde İDK gelişme oranı %53 oranında verilmiştir20. Öte yandan bu oran 10 yılda %28, 24 yılda %36 olarak verildiği başka klinik çalışmalar da bulunmaktadır21,22. Bazı
araştırıcılar DKİS’dan İDK gelişme oranını her yıl için %3 olarak vermektedirler. Burada klinik uygulamalarda akılda tutulması gereken en önemli konu, DKİS lezyonlarının “comedocarcinoma” alt grubunun lezyonun biyolojik davranışındaki agresifliği etkilediğidir. Tarama mammografilerinde saptanan DKİS olgularının %32-50 kadarının “comedocarcinoma” alt bileşeni içerdiği akıldan çıkarılmamalıdır. Bu nedenle DKİS lezyonlarının güvenli takip ve tedavisinde Van Nuys sistemi bizim kliniğimiz de olmak üzere bir çok klinik tarafından standardize edilmiştir.
Tartışılması gereken bir durum da tarama mammografilerinin meme kanserine bağlı ölüm oranının azaltılmasındaki maliyet etkinliğidir. Kırk yaşından başlayarak 79 yaşına kadar yapılan tarama mammografisinin her sağkalınan yıl başına maliyeti 18.800 dolar olarak bulunmuştur. Bu rakam serviks kanseri ve osteoporoz taramalarının aynı şartlardaki maliyeti ile karşılaştırıldığında rakamlar yaklaşık çıkmaktadır. Bu rakam hormon replasman tedavileri, kalp transplantasyonu, hemodiyaliz, koroner arter cerrahisi maliyetlerinden daha azdır23. Öte yandan mammografi ile erken evrede saptanan lezyonların tedavi giderleri daha az olmakta, hastaların adjuvan tedavilerine ait maliyetler düşmekte, iş gücü kaybı azalmakta, hastalık nükslerine ait maliyetler de düşmektedir. Buna bir örnek olarak lokal ileri evre meme kanserlerini verebiliriz. Lokal ileri evre meme kanserleri evre II (T2N1M0, T3N0M0) ve evre IIIA,B,C’yi içermektedir. Maalesef ülkemizde tüm çabalara karşın lokal ileri evre meme
kanseri oranı %15-20 gibi ciddi bir oranda görülmekte, bu da tedavi maliyeti ve sağkalım başarısını olumsuz etkilemektedir. (Resim 1)
Ultrasonografi (USG)
Ultrasonografi 1950 lerden beri kullanıla gelmektedir. Meme hastalıkların tanı ve tedavisinde oldukça değerli bilgiler verebilir. Özellikle fibroglandüler doku yoğunluğunun mammografik incelenin tanısal duyarlığını azalttığı durumlarda daha kesin değerlendirme olanağı sağlar. Meme içindeki kistik ve solid lezyonların ayırıcı tanısında yararlı olduğu gibi, özellikle komplike kistlerin tanı-takip ve tedavisinde yol göstericidir. Ancak DKİS lezyonlarının tanımlanmasında yararı yoktur. Günümüzde yüksek çözünürlüklü ultrasonografik incelemeler solid lezyonların tedavisinde benign-malign ayırımının yapılmasında deneyimli ellerde değerli bilgiler verebilmektedir. Genel olarak USG de saptanan lezyonun elipsoid şekilli olması, hiperekojenitesinin olması, homojen internal ekojenitesinin olması benign kriter olarak kabul edilirken, irregüler kontur varlığı, spiküler patern taşıması, hipoekojenite ve gölgelenme göstermesi de malign kriter olarak kabul edilir. Bununla birlikte 5 mm’den küçük lezyonlarda tanısal kesinliği azalabilmektedir. Ayrıca stromal involusyona uğramış, yağ dokusundan zengin meme dokusunda sağladığı bilgiler incelemeyi yapan radyoloğun deneyimiyle doğru orantılıdır. Ancak USG’de hastanın radyasyona maruz kalmaması, ağrısız bir tetkik olması, eş
zamanlı tanısal girişimlere olanak tanıması (işaretleme, tru cut biyopsi, aspirasyon v.b) değerini
artırmaktadır.
Bilgisayarlı Tomografi (BT) ve Manyetik Rezonans Görüntüleme (MRG)
Her iki tetkikin de kullanılması araştırma konusu olmaya devam etmektedir. Özellikle “fossa axillaris”, mediasten, “fossa supraclavicularisin” içinde muayene ile ele gelmeyen ya da ele gelip de özelliği tam olarak yorumlanamayan lenfadenomegali varlığı hakkında da daha kesin bilgiler vermektedirler. Özellikle son zamanlarda MRG daha yaygın kullanılmaya başlamaktadır. Bir tarama testi olmamasına rağmen, primer tümörlerin tanısında ve lokal nükslerin değerlendirilmesinde yararı görülmektedir. Bir çok klinik çalışmada sensitivite aralığı %88-100 arasında verilmektedir. Öte yandan ailesel meme kanserlerinin tanısında %4 oranında MG ve USG ile saptanmayan lezyonların tanısında yararlıdır. Meme koruyucu cerrahi öncesi “multifocal” ya da “multicentric” lezyonların saptanması cerrahi stratejinin belirlenmesi açısından önem taşır. Bu durumda MRG ameliyat öncesi cerrahi planlamada önemli bilgi verebilmektedir24. Öte yandan profilaktik mastektomi sonrası silikon implant konan hastaların takibinde, mastektomi sonrasında erken rekonstrüksiyon yapılmış hastalarda lokal nükslerin saptanması ve değerlendirilmesinde cerraha yol gösterici olabilmektedir. Daha evvel de
bahsedildiği gibi meme kanserleri sadece “axillar” ve “supraclavicular” metastazlarla da kliniğe
başvurmaktadır. Çoğu kez MG ve USG ile primer lezyonun saptanamadığı “occult carcinoma”
olarak nitelendirilen bu durumda memede primer lezyonun varlığının saptanmasında gadolinium ile yapılan MRG yarar sağlamaktadır. Ayrıca MRG, hastayı iyonize radyasyona maruz bırakmaması, memenin doku yoğunluğundan etkilenmemesi, MG de sadece bir açıdan saptanan lezyonun yerini kesin olarak belirlemesi, bir lezyonun benign-malign ayırımını daha rahat yapması, cerrahi girişim geçirmiş bir memede daha kesin veriler sağlaması yönünden üstünlükler taşır. Bunun yanında klostrofobili kişilerin tetkik zorluğu, maliyeti, mikrokalsifikasyonların değerlendirilmesi güçlüğü ve yöntem standardizasyonu olmaması belli başlı dezavantajlarıdır.
1.2.B. İnvazif tetkikler
Aspirasyon sitolojisi
Aspirasyon biyopsileri 20 gauge iğne kullanılarak şüpheli lezyonun olduğu bölgeden aspire edilen materyalin yayma preparat haline getirilerek incelenmesidir. Materyal elde olunduktan sonra hava etkisi ile kurumaması ve sağlıklı bir sitolojik inceleme yapılması için hemen tespit edilmelidir. Aspirasyon sitolojisin tanısal kesinliği %80 civarındadır. Yanlış negatiflik oranı %18-20 civarında olabilmektedir. Bu nedenle aspire edilen sıvının içşinde malign hücre görülmemesi kanseri ekarte ettirmez. Elde edilen materyal hücresel yapılanmanın bozulmuş olmasından dolayı var olan bir kanser lezyonunda histopatolojik sınıflandırmaya olanak tanımaz. Bunun yanında immünhistokimyasal olarak östrojen, progesteron reseptör tiplemesi de yapılamaz. Bazı merkezlerde meme başına yerleştirlen bir cihaz vakum aspirasyonu sağlanmakta elde edilen sıvıdan tümör belirleyicileri çalışılmaktadır. Özellikle “prostate specific antigen” (PSA) risk saptaması yönünden halen araştırma konusudur.
İğne biyopsisi
Meme konusunda deneyimli bir radyolog tarafından yapılan “tru cut” yöntemi ile yapılan “core needle” biyopsiler daha invazif olmakla birlikte histopatolojik tipleme yapılması ve reseptör çalışmasına olanak tanır. Ayrıca meme koruyucu cerrahi öncesinde cerrahın ameliyat stratjisine de katkıda bulunur. Bu tip biyopsiler steriotaktik olarak ya da USG eşliğinde yapılmaktadır. Kliniğimizde benign lezyon olarak kabul edilmiş fakat aile öyküsü ve tüp bebek tedavisi görmüş bir hastamızda radyolojik değerlendirmedeki şüphe doğrultusunda palpe edilemeyen bir adenofibroma lezyonu içinde daha sonra yapılan işaretli biyopside DKİS lezyonu saptanmıştır (Resim 1).
Açık biyopsi
Bu tip biyopsiler ameliyathane şartlarında eksizyonel biyopsi, insizyonel biyopsi, tel ile işaretlenerek yapılan biyopsiler olmak üzere uygulanabilir. Eksizyonel biyopsi, lezyonun etrafında sağlıklı meme dokusu ile birlikte makroskopik olarak tamamen çıkarılmasıdır. Burada eksizyonel biyopsi yapılırken insizyonun, olası bir definitif cerrahi girişimde uygulanacak insizyon göz önünde tutularak Langer çizgilerine paralel yapılmasına dikkat edilmelidir. İnsizyonel biyopsiler ise daha büyük ve eksize edilemeyecek lezyonlara uygulanır. Burada da yine olası definitif cerrahide uygulanacak insizyon göz önüne alınmalı, sağlıklı reseptör incelemesi için en az 1 ml doku elde edilmesine özen gösterilmelidir. Biyopsi insziyonunun yeri ve büyüklüğünün özellikle meme koruyucu cerrahi uygulanacak hastalarda postoperatif kosmesisi etkileyecek bir durum olduğu akılda tutulmalıdır (Resim 2). Tarama mamografileri bir çok şüpheli lezyonun klinik belirti vermeden saptanmasını olanaklı kıldığı göz önüne
alınırsa. mammografi eşliğinde varlığına karar verilen olası malign lezyon etraf meme dokusuna zarar verilmeden eksize edilmeli, eksize edilen lezyonun tekrar alınan görüntüsü patolojik inceleme ile teyid edilmelidir. İşlem kesinlikle ameliyathane şartlarında yapılması gereken bir uygulamadır. Bu gibi durumlarda lokal anestetik konusunda hastanın cesaretlendirilmesinden kaçınmak gerekir. Çünkü lokal anestetik uygulaması kanlanma paternini etkilemesi yanında dokuda ödeme neden olabileceğinden cerrahi örneklemenin sağlığını olumsuz etkileyebilir.
Meme başı akıntısı yayması
Bazı merkezlerde uygulanmakla birlikte meme başı akıntısından yapılan sitolojik incelemelerin yanlış negatiflik oranı %18, yanlış pozitiflik oranı ise %2.5’tur. Bu nedenle yaygın kullanımı girmiş bir tetkik değildir.
Meme başı biyopsisi, Galaktografi, Duktoskopi
Paget hastalığı, florid papillom gibi lezyonlarda yapılan “wedge” biyopsi uygulamasıdır. Paget hastalığı özellikle areola ve periareoler bölge dahil meme cildindeki her hangi eritamatöz lezyonda akılda tutulmalıdır. Örnekleme yapılırken sadece meme dokusundan değil bu tip lezyonlardan da wedge biyopsi yapılması Paget hastalığına eşlik edebilecek veya neden olabilecek primer lezyonun tanımlanmasında önemli yer tutabileceği gibi eşlik eden lezyonun invaziv kanser dahi olsa meme koruyucu cerrahi uygulama ile başarılı sonuçlar elde edilebilmektedir. Galaktografide ise duktusun birinden kontrast madde enjekte edilmesini takiben alınan mammografilerle duktal ektazi, duktuslarda genişleme ya da dolma defekti saptanmasına çalışılır. Bu tetkik hem uzun sürer hem de tekrarlayan mammografiler çekilmesine gereksinim duyulması nedeniyle dezavantajlıdır. Ayrıca Haagensen serisinde duktustan enjekte edilen radyopak maddenin duktuslardan ektravaze olması memede ciddi iltihabi reaksiyonlara neden olduğu belirtilmektedir. Duktoskopi ve duktal lavaj ise henüz gelişme aşamasındadır. Bununla beraber meme kanseri olgularının %18 den az olmayan oranla
retroareolar bölgede görülüyor olması papillomatöz zeminde gelişebilecek bir tümörün tanısında cerraha önemli sorumluluklar yüklemektedir. Görüntülemede yüksek çözünürlüklü ultrasonografi eşliğnde retroareoler ve peri areoler alanda duktal ektazi saptanması radyolog ve cerrahı uyarmalıdır. Bu gibi durumlarda intraduktal papiller karsinom varlığı akılda tutulmalı wedge biyopsi kararı dikkatle değerlendirilmelidir (Resim 4). Yanısıra, subareoler eksplorasyon kararı ciddi bir zamanlama gerektirebilmektedir.
1.3.Neoplastik gelişimin kinetiği ve interval meme kanseri
Meme kanserinin biyolojik davranışı ile ilgili soruları aydınlatmak için yapılmış geniş hasta gruplarını içeren randomize bir çok tarama amaçlı çalışma mevcuttur. İlk tarama sırasında saptanan kanser prevalansı ile diğer taramada saptanan kanser insidansı arasında geçen zaman meme kanserini oluşturan hücrelerinin büyümesi ve biyolojik aktivitesi ile yakından ilgilidir. Meme kanseri gelişiminin asemptomatik preklinik fazı esnasında prevalans kanserin saptanabildiği mammografi arasında geçen zaman prognoz açısından da son derece önemlidir. Bu zaman bir çok etkenle ilintilidir, bunlar tümör hücrelerinin büyüme paterni, optimal görüntülemenin uygunluğu, radyolog-cerrah-patolog üçlüsünün deneyimi ile ilgilidir. Asemptomatik non-invazif kanser ile asemptomatik invazif kanser arasında geçen zaman “lead time” olarak tanımlanır. Bu “lead time” hastanın sağ kalımını etkileyen bir durum olarak değerlendirilir. Aslında tarama testleri asemptomatik non-invazif tümörün süresini
saptayamamaktadır. Dolayısıyla tarama testleri meme kanseri mortalitesi üzerine sanıldığından
daha etkili de olmayabilir.
Meme kanserinde “lead time” saptamasına yönelik bir çok çalışmalar mevcuttur. Bunlar içerisinde Walter ve Day’in çalışması en rasyonel olarak nitelendirilen çalışmalardandır. Hertarama periyodu için bu süre ortalam 1.7 yıl olarak verilmiştir25.
Meme kanserinde tümör hücrelerin lenfojen yolla yayılması hematojen yayılmasından daha önce olabilmektedir. Hatta hızlı büyüyen tümörlerde “fossa axillaris” lenf nodüllerine metastaz, tümör daha 2-3 mm’lik boyutta iken gerçekleşebilmekte ve 1.5 cm’den daha küçük tümörlerde bile tanı esnasında uzak organ metastazları saptanabilmektedir. Buna karşılık yavaş büyüme paterni gösteren tümörlerde tümör 4-6 cm olsa bile bölgesel ve uzak lenf nodülü metastazları görülmeyebilmektedir. Tarama mammografilerinde bu nedenle amaç asemptomatik noninvazif ya da asemptomatik invazif dönemde bir başka deyişle “lead-time” içerisinde tümörün yakalanmasıdır. Ancak burada “occult” metastazlar olabileceği, tümörün büyüme hızı, histolojik grade, reseptör durumu, bazı özgül genetik belirleyiciler ve “DNA pleudy” durumunun metastazlarda önem kazandığı akılda tutulmalıdır.
Bir çok klinik araştırma negatif mammogram sonrası ikinci bir tarama mammografisi alınmadan interval sırasında gelişen tümör varlığı üzerine odaklanmıştır. Ancak bu şekilde saptanan tümörlerde ikilenme zamanı (İZ) kısa olup metastaz yeteneği daha fazladır. Bu tip tümörlerin tedavisinde tarama sırasında saptanan tümörlere göre daha agresif tedavi yöntemleri planlanması gerekmektedir. İnterval kanserlerde bir diğer problem tarama yapılan hastaların yaş gruplarıyla ilişkisidir. Bu nedenle yapılan araştırmalar gözlenen kanserlerin beklenen kanser sayısına yani interval kanserin oransal insidansına yönelmiştir. Yaş grupları olarak 40-49 ve 50-69 yaşlar olarak ayrılmış ve bu oranların 40-49 yaş arası populasyonda ilk yıl için %62, kinci yıl için %32 bulunmuştur. Aynı oranlar 50-69 yaş populasyon için ilk yıl için %87, ikinci yıl için %71 olarak saptanmıştır26. Ayrıca interval kanserlerin içinde evre II kanser oranı %57.5 olarak bulunmuş ve kontrol grubu ile de farklılık görülmemiştir. Bu çalışmaların sonucunda tarama programına dahil edilen hastalarda saptanan interval kanserlerin prognozu, insidental olarak saptanan aynı evredeki kanserlerden farklı bulunmamıştır. Her ne kadar bu tümörlerin daha kısa İZ’a sahip olmaları yanında, metastaz yeteneği fazla olduğu ifade edilse
de sistemik diseminasyon ve mortalitelerinin tarama dışı hastalara göre yüksek olduğunu gösterecek bir kanıt yoktur.
İnterval kanserlerin mammografik duyarlılığı azaltan bazı histolojik tümör özellikleri olduğu düşünülmüştür. Bu şekilde displastik meme paterni interval kanserlerde %23 olarak bulunmuştur. Bu tümörlerin %15’i lobuler kanser, geri kalan %38’i ise comedo, meduller ve müsinöz kanser olarak rapor edilmiştir27. Ayrıca genç hastalar yaşlı hastalara oranla interval kanser yönünden daha risklidir. Genellikle zayıf ve uzun boylu hastaların interval kanser yönünden daha riskli olduğu düşünülmektedir. Yapay menopoz interval kanser yönünden bir diğer riskli durumdur. İnterval kanserlerin çoğunlukla östrojen reseptörü negatif tümörler olduğu bilinmektedir. Özgeçmişinde benign meme hastalığı öyküsü olan kişilerde daha sık interval meme kanseri saptanmaktadır.
Kaynaklar
1. Haris JR. Breast Cancer, NEngl J Med 327: 319, 1992
2. Courteu JP, Bouchard F. Canadian Natiaonal Breast Screening Study. Can Med Assoc
J 148:875, 1993
3. Mittra I. Breast screening: the case for pyhsical examination without mammography.
Lancet 343, 342, 1994
4. Osteen RT. Breast cancer survey J Am Coll Surg 178:213, 1994
5. Campbell HS. Improving physicians and nurses clinical breast examination: a
randomized conrolled trial. Am J Prev Med 7.1, 1991
6. Wiecha JM, Gann P. Povider confidence in breast examination, Fam Pract Res J. 13:
37, 1993
7. Gadd NA, Souba WW. Evaluation and treatment of benign breast disorders. In Bland
KI, Copeland EM: The Breast Comprehensive management of benign and malign
diseases ed 2, Philadelphia, 1998, WB Saunders.
8. Wanebo HJ. Bilateral breast cancer: risk reduction Ann Surg 201: 667, 1985
9. Goksel HA, Yagmurdur MC, Demirhan B, Isiklar I, Karakayali H, Bilgin N, Haberal
M. Management strategies for patients with nipple discharge. Langenbecks Arch Surg.
390(1):52, 2005
10. Ford D. Genetic heterogeneity and penetrance analysis of the BRCA1 and BRCA2
genes breast cancer families. The bresat cancer linkage consortium. Am J Hum Genet
62: 676, 1998
11. Bays JK.Physical and Mammographic diagnosis of breast cancer and initial work up. J
Am Med Wom Assoc 47: 158, 1992
12. Ng AK, Mauch PM. Second malignancy after Hodgkin’s disease. Am J Oncol Rev
2:190, 2003
13. Göksel HA, Yağmurdur MC. Management of bilateral breast carcinoma: Long term
results. Int Surg 89: 166, 2004
14. Yağmurdur MC, Alevli F. Aberran meme hastalarında kanser insidansı Ulusal Cerrahi
Kongresi 2004 Antalya, Özet Kitap s 71.
15. Feig SA, Hendrick RE. Radiation risk from screening mammography of woman aged
40-49 years. A Monogr Natl Cancer Inst 22: 119, 1997
16. Feig SA. Projected benefits and national health care costs from screening
mammography. Semin Breast Dis 4: 62, 2002
17. Strax P, Venet L, Shapiro S. Value of mammography in reduction of mortality from
breast cancer in mass screening. AJR Am J Roentgenol 117: 686, 1973
18. Duffy SW. Interpretation of the breast screening trials.A commentary on the recent
paper by Gotzsche and Olsen. Breast 10: 209, 2001
19. Feig SA. How eliable is the evidence for screening mammography? Recent results
Cencer Res 163: 129, 2003
20. Feig SA. Ductal carcinoma in situ: implications for screening mammography. Radiol
Clin North Am 38:653, 2000
21. Frykberg ER, Masood S, Copeland EM. Ductal carcinoma in situ of the breast. Surg
Gynecol Obstet 177: 424, 1993
22. Lagios MD. Ductal carcinoma in situ, pathology and treatment. Surg Clin North Am
70:853, 1990
23. Rosenquist CJ, Lindfors KK. Screening mammography beginning at age 40 years. A
repraisal of cost effectiveness Cancer 82:2235, 1998
24. Esserman L. Utility of magnetic resonance imaging in the management of breast cancer:
evidence of improved preoperative staging. J Clin Oncol 17:110, 1999
25. Van Dijck JA. The Current detectability of breast cancer in a mammographic screening
program: a review of the previous mammograms of interval and screen detected cancers.
Cancer 72: 1933, 1993
26. Gilliland F. Biologic characteristics of interval and screen detected breast cancers. J Natl
Cancer Inst 92: 743, 2000
27. Shapiro S. Evidence on screening for breast cancer from a randomized trial. Cancer 39:
2772, 1977
Tablo 1. Meme başı akıntısı nedeniyle başvuran ve biyopsi/subareolar eksplorasyon yapılan hastalarda elde edilen histopatolojik inceleme sonuçları.akıntı karakteri seröz-renkli-kanlı-süt kıvamında olabilir. (SMA: spontan meme başı akıntısı, PMD: provoke meme meme başı akıntısı). (B.Ü.T.F. Dr.Hüsnü Göksel serisi)
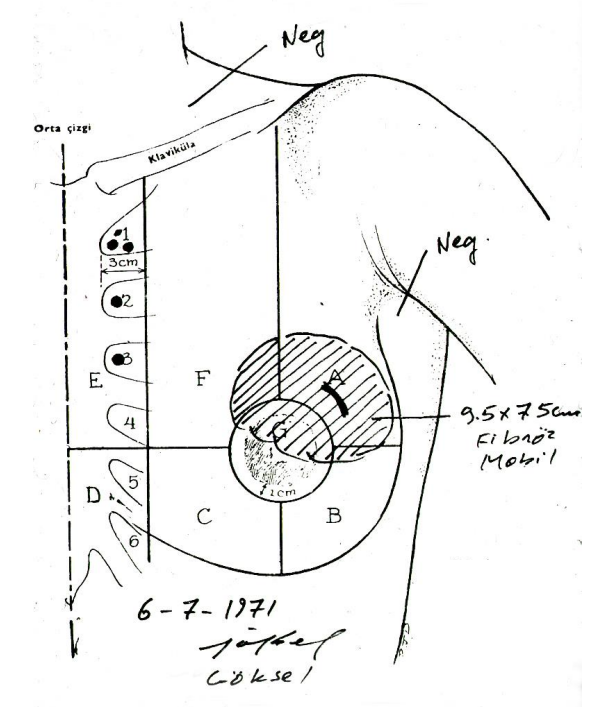
Şekil 1. Meme muayenesi sonrasında kullanılan örnek diyagram
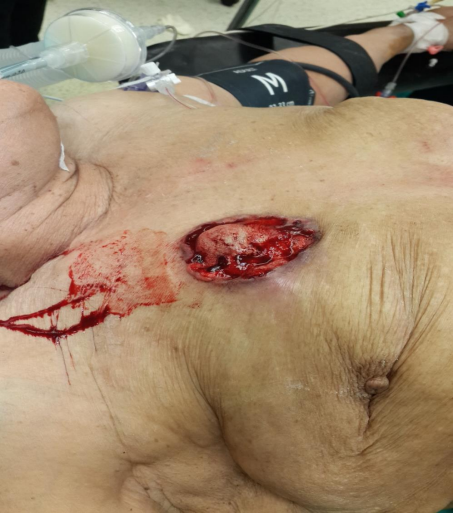
Resim 1. Genellikle Evre 3 B olarak değerlendirilen lokal ileri evre meme kanseri
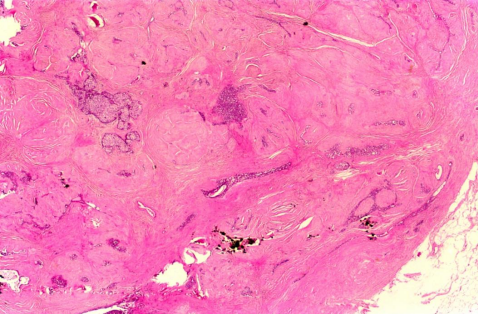
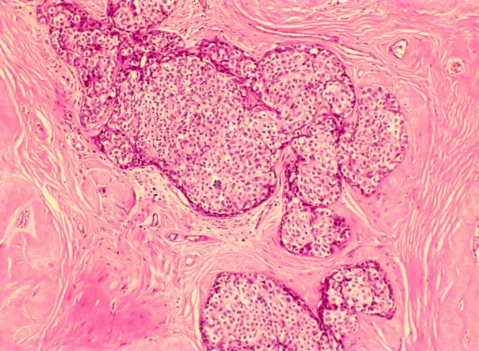
Resim 2. Adenofibroma içerisinde gelişen DKİS lezyonu (Işık mikroskobu x10 ve x40 büyütme)
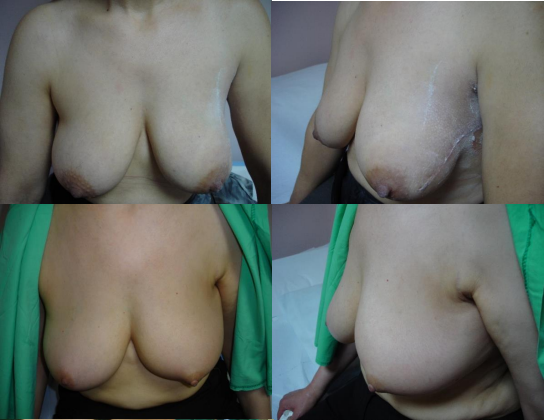
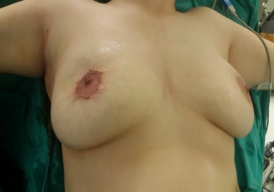
Resim 3. Uygun biyopsi insizyonu uygulandığı takdirde meme koruyucu cerrahi sonrası tatminkar kosmetik sonuca örnekler . (Kadranektomi ve donat mastopeksi ile meme koruyucu cerrahi yapılmış olgular)
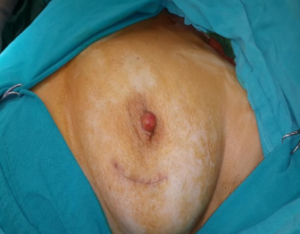
Resim 4. Meme başında Paget invazyonu olgusu